- Строение альдегидов и кетонов. Номенклатура. Изомерия
- Физические свойства альдегидов
- Химические свойства альдегидов
- Получение альдегидов
- Применение альдегидов и кетонов
- рассмотреть особенности строения альдегидов и кетонов
- научиться составлять структурные формулы альдегидов, давать им названия
- научиться составлять уравнения химических реакций с участием альдегидов
- рассмотреть основные способы получения альдегидов
- рассмотреть применение альдегидов
- В какие вещества могут окисляться спирты?
- Что изготавливают из фенолформальдегидной смолы?
- Назовите продукты, получаемые окислением кумола (изопропилбензола) кислородом?
Строение альдегидов и кетонов. Номенклатура
Альдегиды, как и спирты, относятся к кислородсодержащим веществам.
В отличие от спиртов они содержат функциональную группу, в которой кислород соединён с углеродом двойной связью.
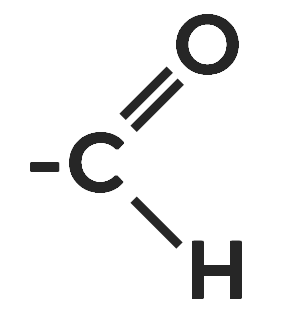
Данная группа в составе альдегидов получила название альдегидной.
Иногда её записывают как Названия альдегидов происходят от названий алканов, только в конце к ним добавляется суффикс аль.
Соответственно, они будут называться: метаналь, этаналь, пропаналь и т. д. Помимо названий по систематической номенклатуре у некоторых альдегидов есть ещё и тривиальные названия, которые приведены в таблице 1.
Таблица 1. Номенклатура альдегидов
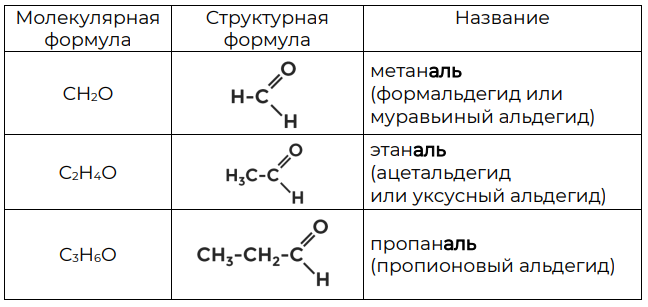
Альдегиды — органические соединения, содержащие альдегидную группу, которая связана атомом водорода или углеводородным радикалом.
Изомерами альдегидов являются очень похожие на них вещества — кетоны. В кетонах углерод функциональной группы соединён с двумя соседними радикалами.
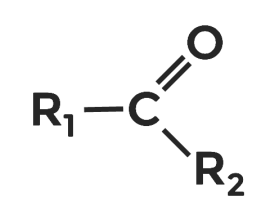
В названии кетонов будет присутствовать суффикс он, например, пропанон или бутанон-2.
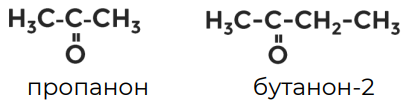
Альдегиды и кетоны вместе образуют карбонильные соединения.
Упражнение 1
Составьте сокращённые структурные формулы: 2-метилпропаналь; 3-метилбутанон-2; 2,3-диметилбутаналь.
Физические свойства альдегидов и кетонов
По агрегатному состоянию альдегиды и кетоны являются летучими жидкостями. В отличие от спиртов у них нет водородных связей между молекулами, поэтому они хуже растворяются в воде и являются более летучими веществам.
Химические свойства альдегидов и кетонов
Альдегиды можно рассматривать как продукты окисления одноатомных спиртов.
Сами же они легко окисляются до карбоновых кислот, поэтому окислительно-восстановительные реакции являются важнейшими для альдегидов.
 Рисунок 1. Осадок оксида меди (I)
Рисунок 1. Осадок оксида меди (I)
Окислительно-восстановительные реакции
Так альдегиды окисляются гидроксидом меди (II), при нагревании превращаясь в карбоновые кислоты (в нашем примере этаналь окисляется в уксусную кислоту). Характерной особенностью реакции является образование осадка кирпично-красного цвета оксида меди (I).
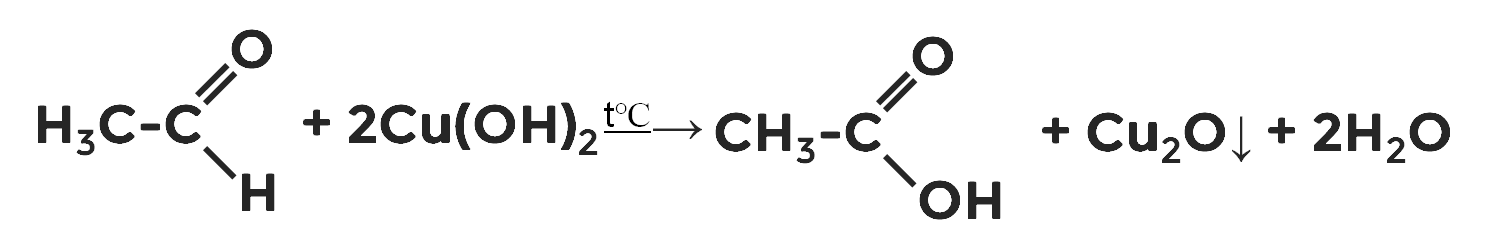
 Рисунок 2. Реакция «серебряного зеркала»
Рисунок 2. Реакция «серебряного зеркала»
Аналогично альдегиды окисляются аммиачным раствором оксида серебра Одним из продуктов реакции является серебро, тонким слоем оседающее на стенках сосуда, напоминая зеркало. Поэтому реакция получила название «реакция серебряного зеркала».

Кетоны окисляются с большим трудом, так как, в отличие от альдегидов, они не могут дать ни карбоновые кислоты, ни их соли.
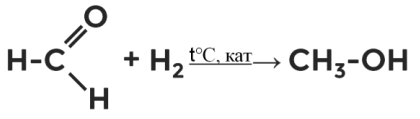
Реакция гидрирования
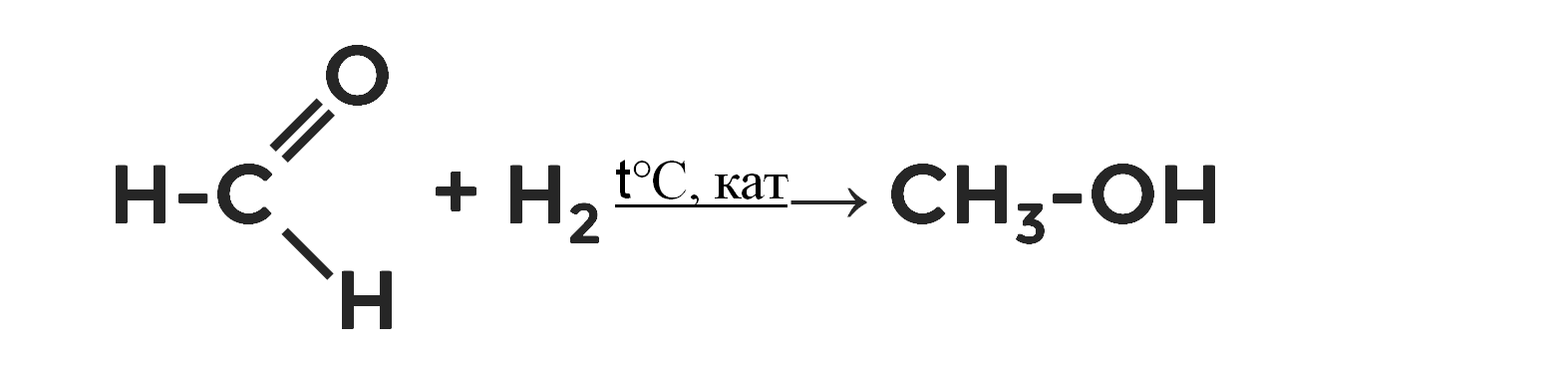
Присоединение водорода является нетипичной реакцией для альдегидов и кетонов. Протекают они под действием высокой температуры и катализаторов. В результате восстановления альдегидов и кетонов водородом образуются
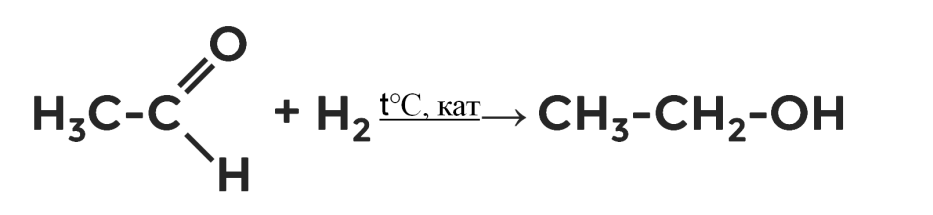
Получение альдегидов и кетонов
1. Окисление спиртов и углеводородов
Вы уже знаете, что спирты окисляются в альдегиды (первичные спирты) или в кетоны (вторичные спирты). Так, формальдегид можно получить окислением спирта метанола кислородом.
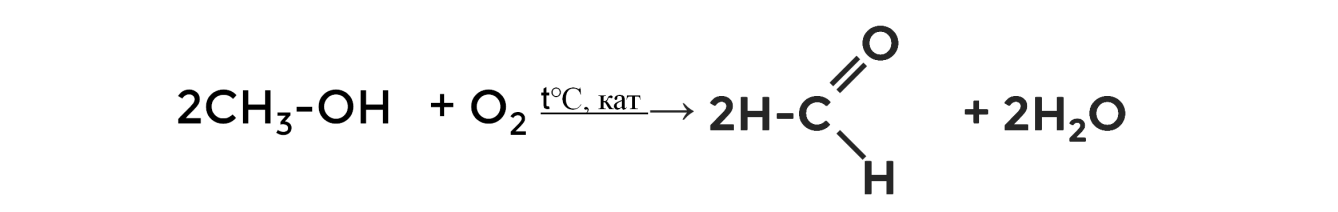
Пропанон, или ацетон, образуется в результате окисления пропанола-2 оксидом меди (II).
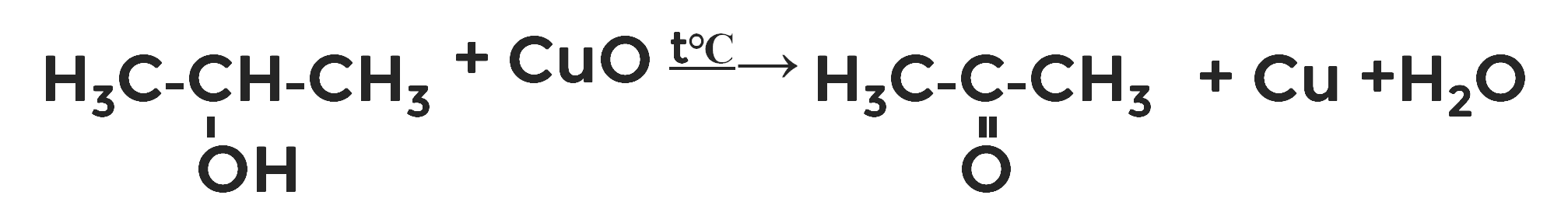
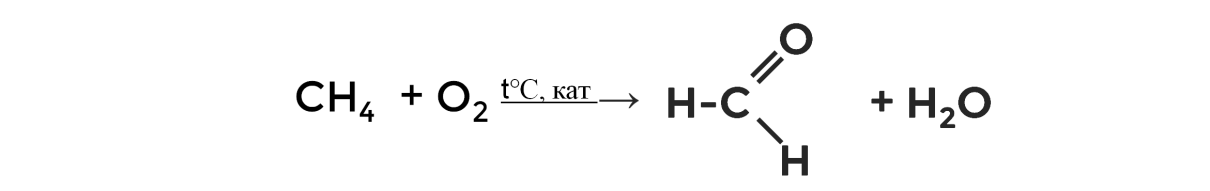
Кроме этого, метаналь в промышленности получают каталитическим окислением метана кислородом.
А этаналь синтезируют окисляя этилен кислородом при высокой температуре на палладиевом катализаторе:
.
2. Гидратация алкинов (реакция Кучерова)
Это знакомая для вас реакция, которую мы изучали в теме «Алкины».
В результате взаимодействия с водой в присутствии солей ртути как катализатора из ацетилена образуется муравьиный альдегид (первая реакция), а из пропина — кетон ацетон или пропанон (вторая реакция).
Применение альдегидов и кетонов
Среди альдегидов наибольшее значение для человека имеют формальдегид и ацетальдегид.
Формальдегид служит сырьём для синтеза фенолформальдегидной смолы, которой пропитывают древесностружечные (и не только) плиты. Смолу получают взаимодействием формальдегида и фенола. В результате реакции образуется полимер и выделяется вода. Поэтому эту и подобные ей реакции относят к реакциям поликонденсации.
Метаналь ядовит. Поэтому его используют для выделки шкур, при хранении анатомических препаратов, кроме того, из него производят лекарственные препараты (рис. 3). Раствор метаналя в воде получил название формалин.
 Рисунок 3. Применение формальдегида
Рисунок 3. Применение формальдегида
Этаналь используется для производства пластмасс, ацетатного волокна, «сухого спирта» (рис. 4). Кетон ацетон, или пропанон, применяется как растворитель органических веществ.
 Рисунок 4. Применение уксусного альдегида
Рисунок 4. Применение уксусного альдегида
Реакция поликонденсации — это реакция образования полимеров, сопровождающаяся отщеплением воды.
Для альдегидов характерна реакция поликонденсации. Так формальдегид вступает в такую реакцию с двумя молекулами фенола.
В результате отщепляется молекула воды и образуется димер — продукт поликонденсации, который носит название фенолформальдегидная смола. Данное соединение широко применяется при производстве клеев и лаков, а также пластмасс.
Упражнение 2
Закончите уравнения химических реакций.
Упражнение 3
Составьте уравнения реакций по схеме.

Формулы веществ записывайте структурно.
Контрольные вопросы
1. В чём особенности строения альдегидов? Что означает «карбонильные соединения»? Какие вещества к ним относятся?
2. Какие химические свойства характерны для альдегидов и кетонов? Почему?
3. Назовите способы получения метаналя и этаналя.
4. Укажите области применения формальдегида.
Ответы
Упражнение 1
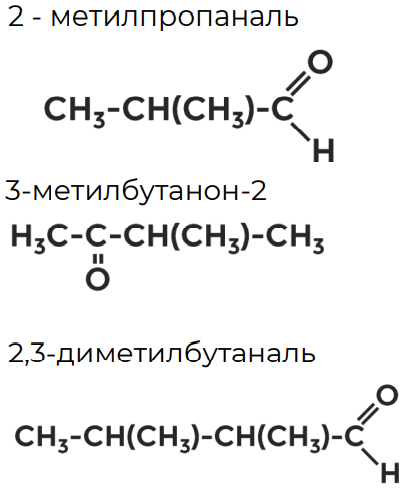
Упражнение 2
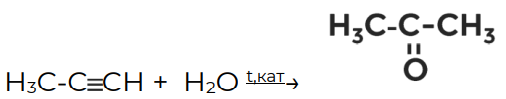
Упражнение 3