- Ионная связь, механизм образования ионной связи
- Понятие «ионы»
- Составление электронных схем образования ионной химической связи
- сформировать понятие об ионной связи, изучить механизм образования ионной химической связи
- познакомиться с понятием «ионы»
- научиться составлять электронные схемы образования химических связей в соединениях с ионным типом связи
- Как изменяется радиус атома в периоде слева направо?
- Как изменяются свойства химических элементов с увеличением порядкового номера в периодах? Почему?
- Как изменяются свойства химических элементов с увеличением порядкового номера в группах (главных подгруппах)? Почему?
Ионная связь, механизм образования ионной связи
Каждый атом химического элемента стремится к завершению своего внешнего электронного слоя (как у инертных газов). При этом из электронейтральных атомов образуются заряжённые частицы — ионы. Из курса физики вы знаете, что разноимённые ионы притягиваются, между ними возникает химическая связь. Следствием является образование вещества.
Ещё древние греки имели представление о том, что такое химическая связь. Древнегреческий мыслитель Эпикур считал, что между атомами существуют некие крючочки, посредством которых атомы удерживались друг с другом. И чтобы «отцепить» один атом от другого, нужно приложить усилие.
Природа химической связи — электростатическая, то есть определяется действием кулоновских сил. Следовательно, причина возникновения связи — стремление атомов к более устойчивому состоянию.
Химическая связь — связь, которая возникает между атомами в молекуле за счёт переноса электронов между этими атомами.
Существует 4 типа связи: ионная, ковалентная, металлическая и водородная.
Ионная химическая связь — связь, которая возникает между ионами за счёт электростатического притяжения.
Эта связь возникает между атомами металлов и неметаллов.
Рассмотрим механизм образования ионной связи.
Составим схемы строения атомов натрия и хлора. Определим число неспаренных электронов на последнем энергетическом уровне.
У атома Na на внешнем энергетическом уровне находится единственный электрон, а у Cl как раз не хватает одного электрона, чтобы его внешний уровень оказался завершённым (8 e-).
Атом металла легко отдаёт свой наиболее удалённый от ядра и слабо связанный с ним электрон атому неметалла, который предоставляет ему свободное место на своём внешнем энергетическом уровне, при этом процессе атомы превращаются в ионы.
Заряд иона определяется количеством отданных или принятых электронов.
Схема образования ионного соединения
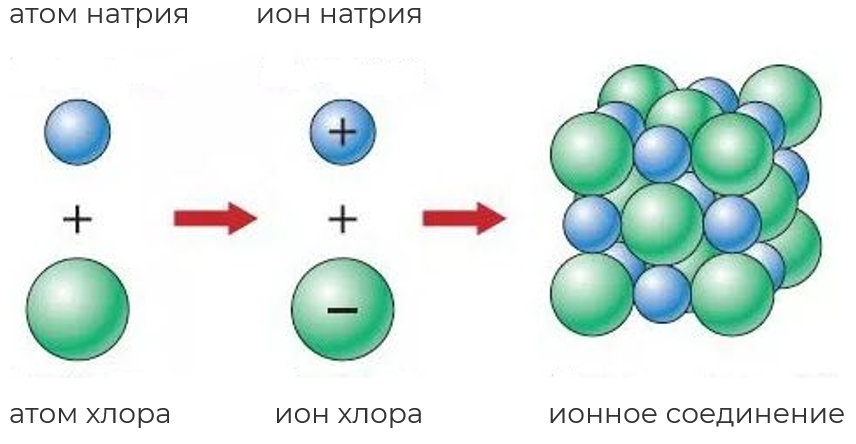 Рис. 1. Схема образования соединения с ионной связью
Рис. 1. Схема образования соединения с ионной связью
Запишем уравнение реакции: .
Цифры, показывающие число атомов или молекул, называют коэффициентами, их ставят перед атомами элементов или перед молекулами. А цифры, показывающие число атомов в молекуле или ионов, — индексами, их ставят в правом нижнем углу, возле атома.
Понятие «ионы»
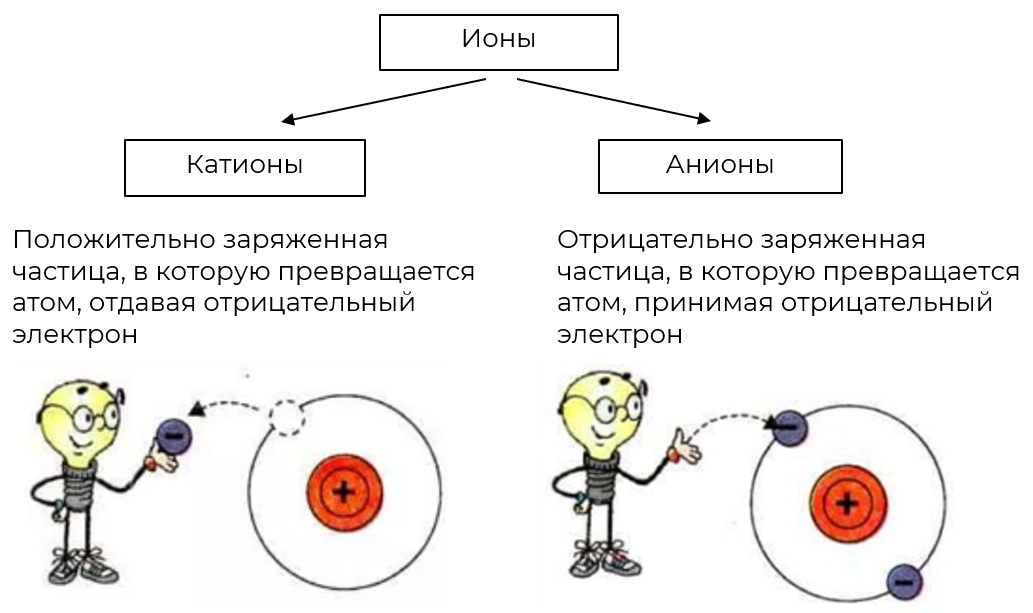
Ионы — частицы, которые образуются в результате перехода электронов от одного атома к другому при образовании химической связи.
Пример 1
Рассмотрим образование ионной связи на примере взаимодействия магния и серы.
Магний для получения устойчивой конфигурации будет отдавать 2 e-, при этом будет превращаться в ион с зарядом 2+.
(катион магния)
Сера для получения устойчивой конфигурации будет присоединять 2 e-, при этом превращаясь в ион с зарядом 2-.
(анион серы)
Таким образом, ионная связь характерна для:
- Оксидов металлов – Na2O, CaO
- Всех солей – LiNO3, FeSO4, CuCl2
- Всех гидроксидов – Са(ОН)2, КОН
- Гидридов металлов – NaH, LiH
Соединения неметалла с ионом NH4+
Упражнение 1
Запишите схему образования связи при взаимодействии натрия с серой.
Контрольные вопросы
- Дайте определение химической связи.
- Что такое ионная связь?
- Атомы каких элементов участвуют в образовании веществ с ионной связью?
Упражнение 1


