- Степень окисления
- Определение степени окисления атомов химических элементов
- Составление химических формул по степени окисления
- сформировать понятие о степени окисления химического элемента
- научиться рассчитывать степени окисления по формулам соединений, а также составлять химические формулы по степени окисления
- Какие типы химической связи вы знаете?
- Что такое электроотрицательность, как она изменяется в периодах, в главных подгруппах?
- Дайте определение ионной связи. Что такое ионы, какие они бывают по заряду?
- Определите тип химической связи для следующих веществ: .
Степень окисления
Когда атомы химических элементов взаимодействуют между собой, образуется химическая связь, электроны между ними в большинстве случаев распределяются неравномерно, поскольку свойства атомов различаются.
Более электроотрицательный атом сильнее притягивает к себе электронную плотность. Атом, который притянул к себе электронную плотность, приобретает частичный отрицательный заряд δ−, а атом, который отдал электроны — частичный положительный заряд δ+. Такие условные заряды называют степенью окисления.
Степень окисления — это условный заряд атомов химического элемента в соединении, вычисленный на основе предположения, что все соединения (и ионные, и ковалентные полярные) состоят из ионов.
Значения степеней окисления ставят над символом элемента арабской цифрой, впереди которой ставят «+» или «−». Например, , степень окисления (+2), (–1).
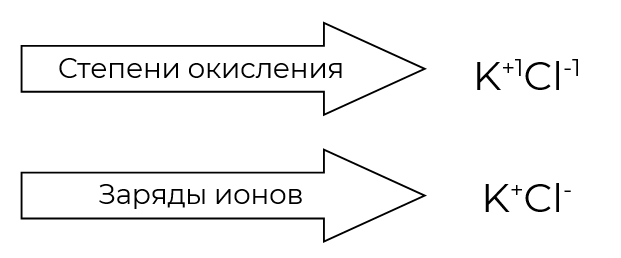
Следует различать степени окисления и заряды ионов. Например, в молекуле , степень окисления (+1), а (−1). В зарядах этих ионов цифры опускают и записывают ионы .
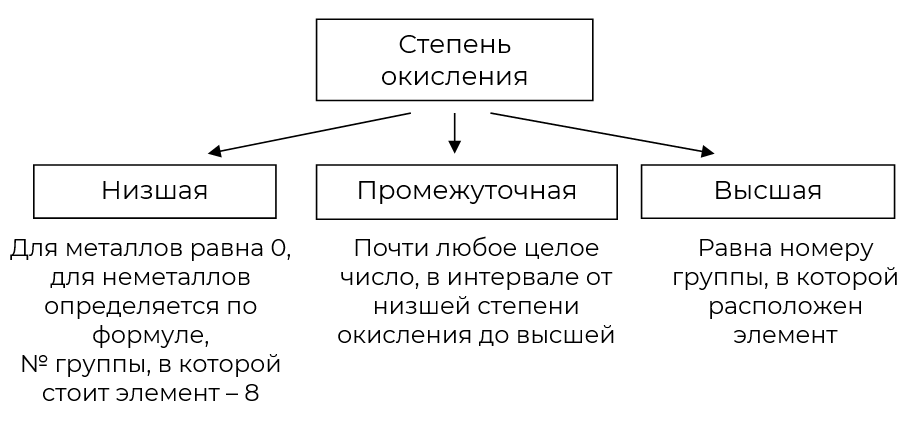
Например, для азота характерны высшая степень окисления +5, низшая 5 − 8 = −3, а промежуточные степени окисления от −3 до +5. Например, в гидразине степень окисления азота промежуточная, −2.
Определение степени окисления атомов химических элементов
Для определения степени окисления пользуются следующими правилами:
- Степень окисления свободных атомов и простых веществ равна 0: ().
- Степень окисления водорода в соединениях с неметаллами равна +1, а с металлами равна −1: ().
- Степень окисления фтора в соединениях всегда равна −1: ().
- Степень окисления кислорода в соединениях равна −2 (), а в пероксидах −1 ().
- Степень окисления металлов в соединениях всегда положительная, у металлов I-A, II-A, III-A соответственно равна +1, +2, +3.
- Суммарная степень окисления всех атомов в молекуле равна 0.
- Элементы в высшей степени окисления могут только принимать электроны.
- Элементы в низшей степени окисления могут только отдавать электроны.
- Элементы в промежуточной степени окисления могут и принимать, и отдавать электроны.
Значения степеней окисления (с. о.) некоторых элементов
|
Постоянная
|
Элемент
|
|
+1
|
в гидридах −1 ()
|
|
+2
|
|
|
+3
|
|
|
−1
|
|
|
−2
|
в пероксидах −1 ()
|
|
Переменная
|
Элемент
|
|
+1, +2
|
|
|
+2, +3
|
|
|
+2, +3, +6
|
|
|
−4, +2, +4
|
|
|
−2, +4, +6
|
|
Алгоритм определения степеней окисления по формуле:
- Определение степеней окисления начинают с того элемента, у которого с. о. постоянная или известна в соответствии с правилами (см. правила): ;
- Умножить эту с. о. на индекс атома (или группы) (–2 · 5 = –10);
- Полученное число разделить на индекс второго элемента (или группы) (10 : 2 = 5);
- Записать полученную c. о. с противоположным знаком ();
- Если вещество состоит из трёх и более элементов, необходимо помнить, что суммарный заряд молекулы равен 0.
Пример 1
Определим степени окисления элементов в бинарном (состоящем из двух элементов) соединении .
Степень окисления нам известна (–2). Следовательно, три атома будут иметь общий заряд (–6), т. к. (–2) · 3 = –6. Тогда общий заряд двух атомов алюминия будет равен (+6). Помните, что суммарный заряд равен 0. Значит, степень окисления одного атома будет (+3), т. к. (+6) : 2 = +3.
Упражнение 1
Определите степени окисления элементов в соединениях:
а) ; б) ; в) ; г) .
Пример 2
Определим степени окисления элементов в соединении, состоящем из трёх элементов .
Степень окисления нам известна (–2), как и степень окисления (+1) Следовательно, четыре атома будут иметь общий заряд (–8), т. к. (–2) · 4 = –8. Общий заряд двух атомов водорода будет равен (+2), т. к. (+1) · 2 = +2.
Мы помним, что суммарный заряд молекулы равен 0. Значит, на один атом серы приходится заряд, равный +6, т. е. степень окисления одного атома будет (+6).
Упражнение 2
Определите степени окисления элементов в соединениях:
а) ; б) ; в) .
Составление химических формул по степени окисления
Алгоритм составления формул по степени окисления:
- Записать знаки элементов (частиц) в порядке: на первом месте — положительно заряженную, на втором — отрицательно заряженную ( );
- Расставить степени окисления ();
- Найти наименьшее общее кратное (НОК) между значениями степеней окисления, записать его между ними в «окошечко»;
- Разделить НОК на значение степеней окисления, полученные результаты записать как индексы (6 : 3 = 2; 6 : 3 = 3 ).
Пример 3
Составим формулу соединения с . Для этого запишем символы элементов ,
. Углерод на втором месте, потому что он более электроотрицательный. — элемент II A группы. Он является металлом, поэтому он отдаст свои 2 электрона и получит степень окисления (+2), а — элемент VII A, он примет 1 электрон для завершения своего внешнего энергетического уровня, на котором уже есть 7 электронов, при этом получит степень окисления (–1). Запишем значения степеней окисления в формулу сверху. Теперь найдём наименьшее общее кратное (НОК). Оно будет 2. Затем НОК разделим на значения степеней окисления и получим соответствующие индексы. 2 : 2 = 1, значит индекс у — 1, 2 : 1 = 2, значит индекс у — 2. Следовательно, формула будет .
Упражнение 3
Составьте формулу соединения:
а) ; б) ; в) .
Контрольные вопросы
- Что такое степень окисления?
- Чему равна степень окисления простых веществ?
- Какой алгоритм составления формулы соединения по степеням окисления элементов?
Упражнение 1
а) ; б); в) ; г) .
Упражнение 2
а) ; б) ; в) .
Упражнение 3
а) ; б) ; в) .

